政策
安徽省發(fā)布新版醫(yī)保藥品目錄:新增415個(gè)藥品
5月16日,安徽省人社廳發(fā)布《安徽省基本醫(yī)療保險(xiǎn)、工傷保險(xiǎn)和生育保險(xiǎn)藥品目錄》(2018年版)通知。新版藥品目錄將于7月1日起執(zhí)行,與原有目錄相比,新增了415個(gè)藥品。
廣州32種藥品納入門診目錄
5月16日,廣州市人社局官網(wǎng)發(fā)布通知,明確將32種藥品納入普通門診藥品目錄、6種藥品納入門慢藥品目錄、7種藥品納入門特藥品目錄。
值得注意的是,這32種藥品囊括了2016年7月首批談判成功的3個(gè)藥品——替諾福韋二吡呋酯、吉非替尼和埃克替尼,以及2017年7月36個(gè)談判品種中的29個(gè)。未納入此次廣州門診目錄的國(guó)家談判品種包括:化藥類的重組人尿激酶原、重組人凝血因子VIIa、重組人腦利鈉肽、利妥昔單抗;中藥類的銀杏二萜內(nèi)酯葡胺注射液、銀杏內(nèi)酯注射液、注射用黃芪多糖。
衛(wèi)計(jì)委發(fā)文:加強(qiáng)兒童等重點(diǎn)人群抗菌藥物臨床應(yīng)用管理
近日,衛(wèi)健委醫(yī)政醫(yī)管局發(fā)布《關(guān)于持續(xù)做好抗菌藥物臨床應(yīng)用管理有關(guān)工作的通知》國(guó)衛(wèi)辦醫(yī)發(fā)〔2018〕9號(hào),要求進(jìn)一步加強(qiáng)抗菌藥物臨床應(yīng)用管理。《通知》特別明確:加強(qiáng)兒童等重點(diǎn)人群抗菌藥物臨床應(yīng)用管理。
新藥
FDA批準(zhǔn)首個(gè)預(yù)防偏頭痛新藥
近日,美國(guó)FDA批準(zhǔn)了安進(jìn)公司的Aimoving(erenumab-aooe)作為成人偏頭痛的預(yù)防性治療,給藥方式為每月一次注射。值得一提的是,Aimoving是FDA批準(zhǔn)的第一個(gè)預(yù)防性偏頭痛治療藥物,通過(guò)阻斷降鈣基因相關(guān)肽的活性發(fā)揮作用。
恒瑞醫(yī)藥磺達(dá)肝癸鈉注射液獲美國(guó)FDA批準(zhǔn)
5月18日,恒瑞醫(yī)藥發(fā)布公告稱,公司已收到美國(guó)FDA通知,其申報(bào)的磺達(dá)肝癸鈉注射液簡(jiǎn)略新藥申請(qǐng)(ANDA)已獲得批準(zhǔn),意味著恒瑞可以生產(chǎn)并在美國(guó)市場(chǎng)銷售該產(chǎn)品。2009 年,英國(guó) Glaxo Group Ltd 的磺達(dá)肝癸鈉注射液在中國(guó)獲批上市,至今,國(guó)內(nèi)暫無(wú)內(nèi)資企業(yè)獲批,但除恒瑞醫(yī)藥外,國(guó)內(nèi)另有正大天晴、天津紅日、信泰制藥、遼寧海思科等多家企業(yè)提交了6 類申請(qǐng)。
FDA批準(zhǔn)首個(gè)非阿片類戒斷新藥
近日,美國(guó)FDA宣布,批準(zhǔn)US WorldMeds的Lucemyra(鹽酸洛非斯汀)用于緩解突然停用阿片類藥物的成人患者戒斷癥狀,該治療最長(zhǎng)用藥時(shí)間為14天。Lucemyra是一種口服選擇性α2-腎上腺素受體激動(dòng)劑,可減少去甲腎上腺素的釋放。
首個(gè)Epogen生物仿制藥獲FDA批準(zhǔn)
近日,美國(guó)FDA宣布,批準(zhǔn)輝瑞旗下Hospira的Retacit作為Epogen的生物仿制藥,用于治療由慢性腎病、化療或使用齊多夫定治療HIV感染而導(dǎo)致的貧血癥。
FDA批準(zhǔn)UCB公司的抗癲癇藥物新適應(yīng)癥
5月15日,總部位于比利時(shí)的生物醫(yī)藥公司UCB宣布,美國(guó)FDA已經(jīng)批準(zhǔn)了該公司最新的抗癲癇藥物BRIVIACT?(brivaracetam布力西坦)口服制劑的補(bǔ)充新藥申請(qǐng)(sNDA),用于單獨(dú)或輔助治療4歲及以上患者的局部癲癇發(fā)作(partial-onset seizure,POS)。此前,F(xiàn)DA曾批準(zhǔn)BRIVIACT?用于單獨(dú)或輔助治療16歲及以上患者的POS。
上海醫(yī)藥腫瘤藥SPH3348片劑獲臨床批件
5月17日,上海醫(yī)藥發(fā)布公告稱,公司及其全資子公司上海醫(yī)藥集團(tuán)(本溪)北方藥業(yè)有限公司開(kāi)發(fā)的“SPH3348 片”獲得國(guó)家食品藥品監(jiān)督管理總局頒發(fā)的藥物臨床試驗(yàn)批件。該藥物為選擇性抑制劑,具有抗腫瘤作用,用于非小細(xì)胞肺癌(NSCLC)等惡性腫瘤的治療。該藥物國(guó)內(nèi)外尚無(wú)同類產(chǎn)品獲批上市。
企業(yè)
阿里健康2018財(cái)年收入增長(zhǎng)超400% 首次扭虧為盈
5月16日,阿里健康發(fā)布了2018年業(yè)績(jī)公告(截止2018年3月31日),報(bào)告期內(nèi),集團(tuán)實(shí)現(xiàn)收入約24.43億元(人民幣,下同),同比增長(zhǎng)414.2%;毛利6.53億元,同比增長(zhǎng)248.7%。值得注意的是,若扣除股權(quán)激勵(lì)費(fèi)用約1.17億元,則經(jīng)調(diào)整利潤(rùn)達(dá)800萬(wàn)元,而上一財(cái)年則為經(jīng)調(diào)整虧損9832.9萬(wàn)元,首次實(shí)現(xiàn)扭虧為盈。
正大天晴的恩替卡韋分散片通過(guò)一致性評(píng)價(jià)
5月15日,中國(guó)生物制藥控股的正大天晴藥業(yè)申請(qǐng)的恩替卡韋分散片(商品名:潤(rùn)眾)通過(guò)一致性評(píng)價(jià)審核,從申請(qǐng)受理到獲批歷經(jīng)了10個(gè)月的時(shí)間。恩替卡韋由中美上海施貴寶公司在2005年引入中國(guó)市場(chǎng),商品名為“博路定”,其是治療乙型肝炎的一線藥物。
嘉林藥業(yè)的阿托伐他汀鈣片通過(guò)一致性評(píng)價(jià)
5月15日,德展大健康發(fā)布上市公司公告,稱其全資子公司北京嘉林藥業(yè)股份有限公司已于今日收到國(guó)家食品藥品監(jiān)督管理總局核準(zhǔn)簽發(fā)的化學(xué)藥品“阿托伐他汀鈣片”的《藥品補(bǔ)充申請(qǐng)批件》。這意味著其核心品種“阿樂(lè)”已經(jīng)正式通過(guò)仿制藥質(zhì)量和療效一致性評(píng)價(jià)。
]]>
1.《良好ANDA提交規(guī)范》草案:公開(kāi)仿制藥申報(bào)資料常見(jiàn)缺陷并提出建議
目前,一個(gè)仿制藥獲得批準(zhǔn)前,平均要經(jīng)過(guò)4輪審評(píng),主要是因?yàn)樯暾?qǐng)材料中缺乏必需信息或證據(jù)不充分,不得不要求申請(qǐng)人補(bǔ)充資料。該行業(yè)指南草案旨重點(diǎn)闡述了可能導(dǎo)致ANDA審批延遲的常見(jiàn)缺陷,以及針對(duì)申請(qǐng)人如何規(guī)避這些缺陷、如何回復(fù)的建議。主要探討的缺陷包括:
* 專利和專營(yíng)權(quán)缺陷
* 標(biāo)簽缺陷
* 產(chǎn)品質(zhì)量缺陷
* 生物等效性缺陷
2.《良好ANDA評(píng)估實(shí)踐規(guī)范》:規(guī)范評(píng)價(jià)行為,以評(píng)估(assessment)替代審評(píng)(review),對(duì)缺陷闡釋更為清晰
這是一份政策和程序文件(Manual of Policy and Procedure,MAPP)。MAPP是描述FDA工作人員如何開(kāi)展工作的文件,MAPP的公布是為了向行業(yè)提供更大的透明度。這份MAPP是用于規(guī)范仿制藥審評(píng)、提高工作效率和有效性的工作手冊(cè),主要目標(biāo)是減少審評(píng)的輪次,提高批準(zhǔn)率,加速批準(zhǔn)符合要求的仿制藥。
OGD和OPQ將使用術(shù)語(yǔ)“評(píng)價(jià)(assessment)”替代“審評(píng)(review)”。此次的MAPP中給出了“評(píng)估”的定義,但未說(shuō)明它與審評(píng)的區(qū)別:評(píng)估是指對(duì)提交的數(shù)據(jù)和信息進(jìn)行評(píng)價(jià)和分析,以決定該申請(qǐng)是否符合批準(zhǔn)要求并記錄該決定的過(guò)程。
該MaPP的重點(diǎn)內(nèi)容包括:
* 引入新的審評(píng)模板,使每輪審評(píng)更加高效和完整。
* 簡(jiǎn)化仿制藥審評(píng)流程,由過(guò)去的一級(jí)、二級(jí)和三級(jí)審評(píng)改為僅進(jìn)行一級(jí)、二級(jí)評(píng)估,不再進(jìn)行三級(jí)評(píng)估。明確各級(jí)審評(píng)人員的職責(zé),其中部門主任不再進(jìn)行審評(píng),只是管理內(nèi)部工作,確保遵守實(shí)踐規(guī)范,并接受審評(píng)員的咨詢。
* 如ANDA申請(qǐng)不能獲得批準(zhǔn),審評(píng)人員應(yīng)更詳細(xì)地向申請(qǐng)人解釋申請(qǐng)資料中的缺陷,并具體說(shuō)明需要何種補(bǔ)充信息、應(yīng)如何提高補(bǔ)充信息。其目的在于使申請(qǐng)人充分了解其批準(zhǔn)延遲的問(wèn)題,以及如何糾正并再次申請(qǐng),從而減少后續(xù)的審評(píng)輪次。
FDA期望通過(guò)發(fā)布和實(shí)施這兩份文件以及更多措施,在2018年能夠促進(jìn)藥品競(jìng)爭(zhēng)、幫助降低藥價(jià)、擴(kuò)大藥品可及性。
]]>自公告發(fā)布之日起,對(duì)已由省級(jí)藥品監(jiān)管部門受理并正在國(guó)家藥品監(jiān)督管理局審評(píng)審批的化學(xué)仿制藥注射劑注冊(cè)申請(qǐng),國(guó)家藥品監(jiān)督管理局將加大有因檢查的力度,國(guó)家食品藥品監(jiān)督管理總局藥品審評(píng)中心(以下簡(jiǎn)稱藥審中心)在嚴(yán)格審評(píng)的基礎(chǔ)上,根據(jù)審評(píng)需要提出現(xiàn)場(chǎng)檢查需求,由國(guó)家食品藥品監(jiān)督管理總局食品藥品審核查驗(yàn)中心(以下簡(jiǎn)稱核查中心)實(shí)施現(xiàn)場(chǎng)檢查。
五種情況需現(xiàn)場(chǎng)檢查
1.注射劑的處方、工藝、內(nèi)包材、生產(chǎn)設(shè)備發(fā)生變更,屬于《已上市化學(xué)藥品變更研究的技術(shù)指導(dǎo)原則(一)》《已上市化學(xué)藥品生產(chǎn)工藝變更研究技術(shù)指導(dǎo)原則》規(guī)定的Ⅲ類變更或重大變更的情形的。
2.國(guó)產(chǎn)制劑的生產(chǎn)地點(diǎn)(生產(chǎn)線)發(fā)生變更的。
3.首次申報(bào)化學(xué)藥注射劑型,相應(yīng)生產(chǎn)線尚未生產(chǎn)過(guò)其他品種的。
4.審評(píng)過(guò)程發(fā)現(xiàn)真實(shí)性存疑等需要核實(shí)的。
5.收到真實(shí)性和可靠性問(wèn)題投訴舉報(bào)線索需要核實(shí)的。
檢查重點(diǎn)
核查中心將根據(jù)審評(píng)需要對(duì)化學(xué)仿制藥注射劑注冊(cè)申請(qǐng)開(kāi)展現(xiàn)場(chǎng)檢查,并通知注冊(cè)申請(qǐng)人。檢查重點(diǎn)包括注冊(cè)申請(qǐng)人整體實(shí)施藥品生產(chǎn)質(zhì)量管理規(guī)范水平與申報(bào)品種無(wú)菌保證能力,以及品種申報(bào)時(shí)動(dòng)態(tài)生產(chǎn)批次情況,包括生產(chǎn)批量等與申報(bào)資料的一致性、真實(shí)性等相關(guān)內(nèi)容。必要時(shí),核查中心可要求注冊(cè)申請(qǐng)人在檢查期間安排動(dòng)態(tài)生產(chǎn)和抽樣檢驗(yàn)。
屬于上述第1和第2種情況的,待審評(píng)結(jié)束后,藥審中心不再通知省級(jí)藥品監(jiān)管部門重復(fù)進(jìn)行生產(chǎn)現(xiàn)場(chǎng)檢查。
公告指出,注冊(cè)申請(qǐng)人發(fā)現(xiàn)相關(guān)化學(xué)仿制藥注射劑注冊(cè)申請(qǐng)內(nèi)容存在不真實(shí)、不完整等問(wèn)題的,可以在核查中心通知現(xiàn)場(chǎng)檢查前申請(qǐng)撤回。通知現(xiàn)場(chǎng)檢查后不再接受撤回申請(qǐng)。對(duì)現(xiàn)場(chǎng)檢查發(fā)現(xiàn)存在真實(shí)性問(wèn)題甚至弄虛作假的,將依法嚴(yán)肅查處。
]]>
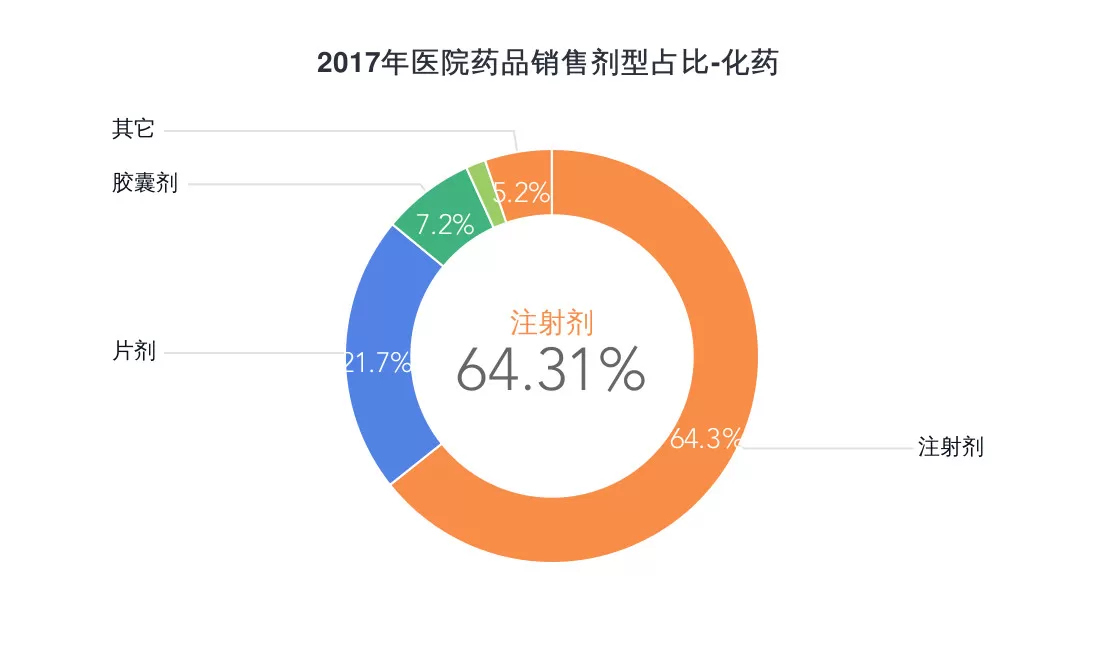
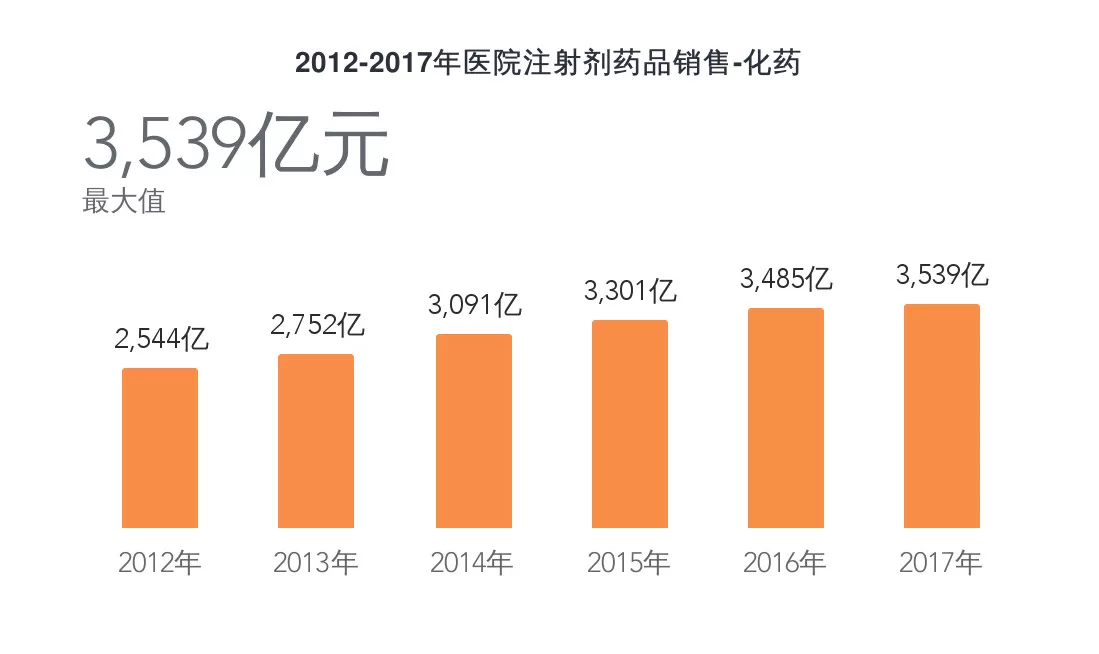
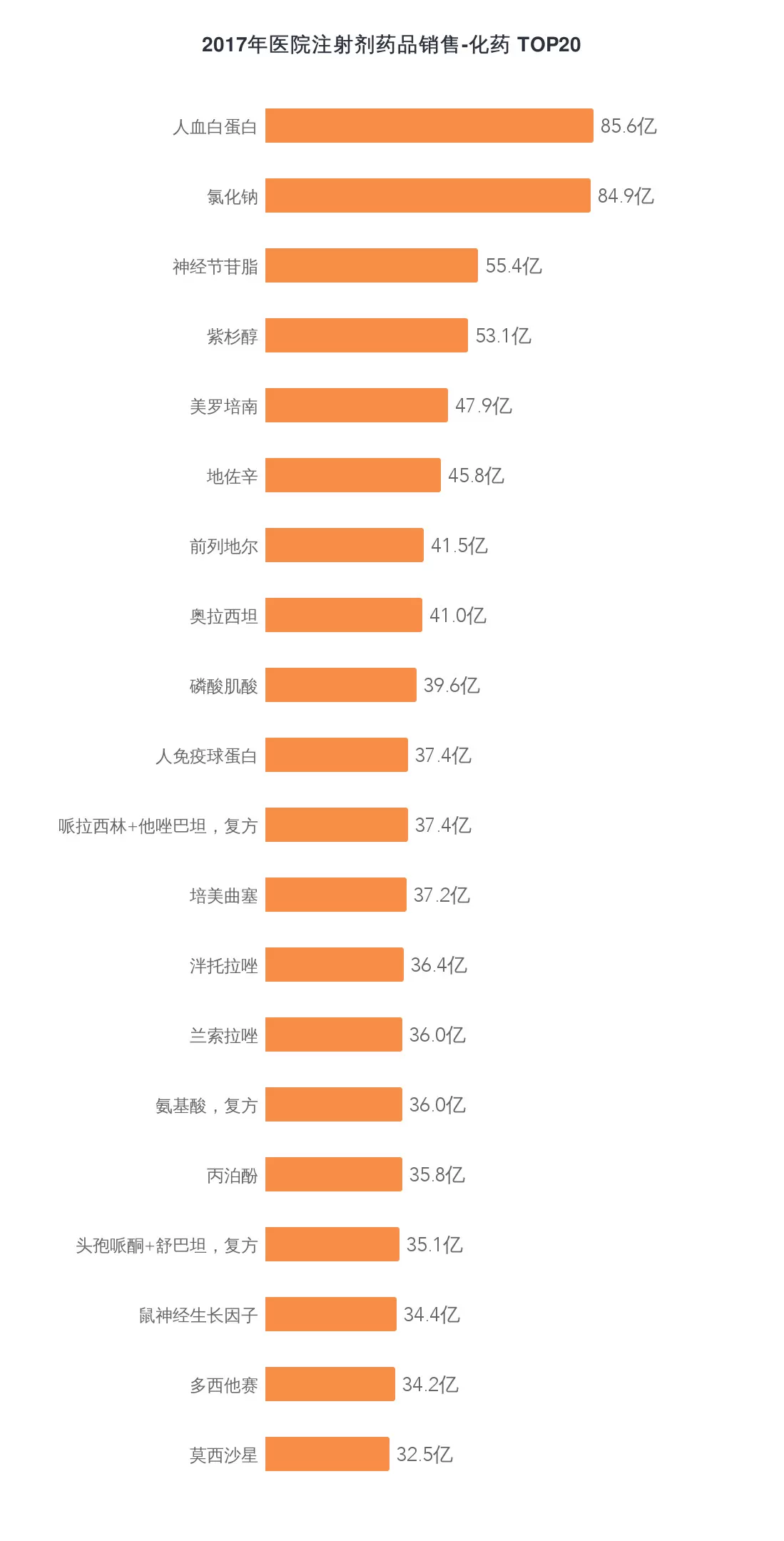
數(shù)據(jù)說(shuō)明:
1、銷售數(shù)據(jù)根據(jù)醫(yī)院采購(gòu)、上市公司年報(bào)等信息測(cè)算得出。
2、注射劑包括注射液、粉針劑、特殊注射給藥劑型。
]]>
▍正大天晴:鹽酸安羅替尼(福可維),企業(yè)的里程碑
5月14日,國(guó)家藥監(jiān)局發(fā)布消息:治療非小細(xì)胞肺癌新藥,鹽酸安羅替尼膠囊(福可維)獲批上市。
據(jù)了解,“福可維”是正大天晴藥業(yè)集團(tuán)自主研發(fā)的1.1類新藥。其團(tuán)隊(duì)歷經(jīng)10年10余年的努力,在腫瘤藥物的開(kāi)發(fā)上取得了突破。安羅替尼上市,是正大天晴發(fā)展史上里程碑式的事件。
這一產(chǎn)品是新型小分子多靶點(diǎn)酪氨酸激酶抑制劑,能有效抑制VEGFR、PDGFR、FGFR、c-Kit等激酶,具有抗腫瘤血管生成和抑制腫瘤生長(zhǎng)的雙重功效。
“福可維”是目前晚期非小細(xì)胞肺癌抗血管生成靶向藥物中,僅有的單藥有效的口服制劑,而且不良反應(yīng)較輕,患者耐受性良好。業(yè)內(nèi)專家分析,安羅替尼有望成為晚期非小細(xì)胞肺癌患者三線治療的標(biāo)準(zhǔn)用藥。
▍拜耳:艾力雅,2月獲批上市,5月增加適應(yīng)癥
5月10日,拜耳公司宣布,國(guó)家藥品監(jiān)督管理局已批準(zhǔn)艾力雅(阿柏西普眼內(nèi)注射溶液)用于治療成人新生血管(濕性)年齡相關(guān)性黃斑變性(nAMD)。國(guó)家藥品監(jiān)督管理局藥品審評(píng)中心(CDE)于2017年6月將該上市申請(qǐng)納入優(yōu)先審評(píng)程序。
在2018年2月13日,總局批準(zhǔn)“艾力雅”用于治療成人糖尿病性黃斑水腫(DME)上市。
目前,阿柏西普眼內(nèi)注射溶液已有五個(gè)適應(yīng)癥在全球100多個(gè)國(guó)家獲準(zhǔn)上市。全球范圍內(nèi)使用量已超過(guò)2000萬(wàn)支。
▍正大天晴:醋酸加尼瑞克注射液,國(guó)內(nèi)首仿
5月2日,中國(guó)生物制藥宣布,子公司正大天晴開(kāi)發(fā)的藥物醋酸加尼瑞克注射液(晴樂(lè))已獲批在國(guó)內(nèi)上市,成為該產(chǎn)品的國(guó)內(nèi)首仿藥。
“晴樂(lè)”是輔助生殖領(lǐng)域的降調(diào)藥,屬于促性腺激素釋放激素(GnRH)類似物。其適應(yīng)癥為在接受輔助生殖技術(shù)控制性卵巢刺激方案的婦女中使用,可預(yù)防過(guò)早出現(xiàn)促黃體激素(LH)峰。
隨著中國(guó)人口生育年齡的增長(zhǎng)以及二胎政策的放開(kāi),需要接受輔助生殖治療的女性將會(huì)越來(lái)越多。“晴樂(lè)”有望成為原研“歐加利”的有力競(jìng)品。
▍默沙東:9價(jià)HPV疫苗,8天獲批
4月28日,國(guó)家藥品監(jiān)督管理局有條件批準(zhǔn),用于預(yù)防宮頸癌的默沙東9價(jià)HPV疫苗(佳達(dá)修)上市。4月20日,默沙東的上市申請(qǐng)獲CDE承辦受理。只用了8天,獲批。
5月11日,在海南進(jìn)行了掛網(wǎng)價(jià)格談判,談判價(jià)格為1298元/支。
相關(guān)數(shù)據(jù)顯示,2016年全球HPV疫苗市場(chǎng)規(guī)模達(dá)22.8億美元,其中,默沙東的佳達(dá)修(四價(jià)+九價(jià))疫苗銷售額為21.7億美元,市場(chǎng)份額超過(guò)95%,處于絕對(duì)壟斷地位。
據(jù)中國(guó)證券網(wǎng)報(bào)道,目前已有三家企業(yè)獲批九價(jià)HPV疫苗的臨床批件,積極開(kāi)展臨床試驗(yàn)。分別是沃森生物子的公司——上海澤潤(rùn),以及廈門萬(wàn)泰和上海博唯。
▍默沙東:艾爾巴韋格拉瑞韋片——“化學(xué)英雄”
5月8日,默沙東公司宣布,其慢性丙型肝炎口服直接抗病毒藥物,艾爾巴韋格拉瑞韋片固定劑量復(fù)方制劑于,2018年4月28日獲得國(guó)家藥品監(jiān)督管理局(原國(guó)家食品藥品監(jiān)督管理總局)的上市批準(zhǔn),適用于治療基因1、4型慢性丙肝的成年患者。
此次獲批的艾爾巴韋格拉瑞韋片,是由默沙東攜手藥明康德共同參與研發(fā),雙方還共同榮膺2017美國(guó)化學(xué)學(xué)會(huì)“化學(xué)英雄”獎(jiǎng)。此外,艾爾巴韋格拉瑞韋片還曾被美國(guó)FDA兩次授予“突破療法認(rèn)證”。
▍阿斯利康:百達(dá)揚(yáng)上市,三生制藥代理20年
1月4日,三生制藥發(fā)布公告,一款能夠?qū)崿F(xiàn)一周一次給藥的降糖藥物,獲國(guó)家食藥監(jiān)總局批準(zhǔn)上市。這是一款胰高血糖素樣肽-1(GLP-1)受體激動(dòng)劑周制。商品名是百達(dá)揚(yáng)(Bydureon),通用名是注射用艾塞那肽微球,用于2型糖尿病治療。
目前,GLP-1受體激動(dòng)劑周制劑已在美國(guó)、歐洲、日本、韓國(guó)、香港、臺(tái)灣等多地上市。此次上市的“百達(dá)揚(yáng)”被認(rèn)為是中國(guó)首個(gè),一周一次給藥的胰高血糖素樣肽-1藥物。
這個(gè)藥由阿斯利康研發(fā),2017年10月11日,三生制藥發(fā)公告,以1億美元,獲此系列藥物在中國(guó)的獨(dú)家商業(yè)權(quán),有效期20年。
▍西安楊森:欣普尼——抗風(fēng)濕生物制劑
1月4日,西安楊森制藥宣布,國(guó)家食藥監(jiān)總局已經(jīng)批準(zhǔn)“欣普尼”(SIMPONI),即戈利木單抗注射液。用于治療活動(dòng)性強(qiáng)直性脊柱炎成年患者;也可聯(lián)合甲氨蝶呤(MTX)治療對(duì)MTX在內(nèi)的改善病情抗風(fēng)濕藥物療效不佳的中到重度活動(dòng)性類風(fēng)濕關(guān)節(jié)炎成年患者。
“欣普尼”是全人源化抗腫瘤壞死因子(TNF-alpha)單克隆抗體,是中國(guó)首個(gè)獲批的每月皮下注射一次的抗風(fēng)濕生物制劑。目前,已在94個(gè)國(guó)家獲批。
▍恒瑞:硫培非格司亭注射液,即將上市
據(jù)報(bào)道,5月8日,國(guó)家藥品監(jiān)督管理局網(wǎng)站信息顯示,恒瑞重磅品種硫培非格司亭注射液(聚乙二醇重組人粒細(xì)胞刺激因子注射液,19K)上市申請(qǐng)(CXSS1700005)的審批狀態(tài)已經(jīng)變更為“審批完畢-待制證”。
是國(guó)內(nèi)外臨床指南首推的用于放化療相關(guān)中性粒細(xì)胞減少癥治療藥物,包括短效和長(zhǎng)效兩種類型。據(jù)知情人透露,該品種已獲得批準(zhǔn)上市。
分析師預(yù)測(cè),這個(gè)產(chǎn)品銷售峰值可達(dá)20億元。國(guó)內(nèi)目前已經(jīng)有近20家企業(yè)生產(chǎn)短效G-CSF藥物,但上市的長(zhǎng)效G-CSF藥物僅有百克生物的津優(yōu)力和齊魯制藥的新瑞白兩家。
]]>
制銷售和控制類的藥品,因?yàn)楂@取的過(guò)程,手續(xù)復(fù)雜,費(fèi)用昂貴,不屬于本文的討論范圍內(nèi)。本文討論的是最普通的沒(méi)有任何限制銷售的藥品,拿下面美國(guó)3個(gè)最暢銷的藥品作為例子,我們來(lái)探討一下為什么美國(guó)的參比制劑價(jià)格超貴,以及美國(guó)病人是如何來(lái)承受這樣天價(jià)的藥品的。
首先,美國(guó)藥品保險(xiǎn)公司,給美國(guó)病人都會(huì)有很大的折扣,即使沒(méi)有保險(xiǎn)的病人,美國(guó)藥房,網(wǎng)上,到處都可以找到打折的卡。美國(guó)藥品的標(biāo)價(jià),對(duì)于美國(guó)的病人來(lái)說(shuō)是沒(méi)有意義的,因?yàn)椴∪硕紩?huì)有非常大的折扣的,比如,50%左右(見(jiàn)下面的3個(gè)例子)。參比制劑是用于出口的,沒(méi)有這個(gè)保險(xiǎn)公司的折扣。
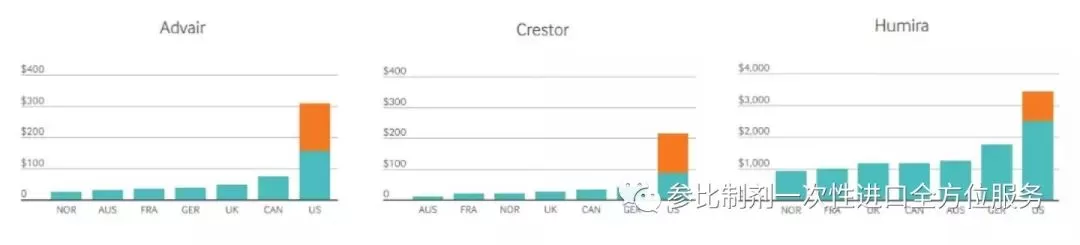
從上面3個(gè)藥品的價(jià)格數(shù)據(jù)看到,美國(guó)的藥品價(jià)格是全世界最貴的。歐洲不同國(guó)家的價(jià)格,價(jià)格也不同。加拿大德國(guó)已經(jīng)慢慢成為藥品第二貴的國(guó)家了。
例1,ADVAIR每個(gè)月的價(jià)格,美國(guó)不經(jīng)過(guò)保險(xiǎn)公司折扣的價(jià)格是309.6 美元,美國(guó)經(jīng)過(guò)保險(xiǎn)公司的折扣后的價(jià)格154.8美元,全球第二貴的國(guó)家,加拿大的價(jià)格是74.12美元。如果國(guó)內(nèi)采購(gòu)美國(guó)的參比制劑,就要以309.6美元為起點(diǎn),加上中間供應(yīng)商轉(zhuǎn)手的利潤(rùn),運(yùn)費(fèi),等。
例2,CRESTOR每個(gè)月的價(jià)格,美國(guó)不經(jīng)過(guò)保險(xiǎn)公司折扣的價(jià)格是216 美元,美國(guó)經(jīng)過(guò)保險(xiǎn)公司的折扣后的價(jià)格86.4美元,全球第二貴的國(guó)家,德國(guó)的價(jià)格是40.5美元。如果國(guó)內(nèi)采購(gòu)美國(guó)的參比制劑,就要以216美元為起點(diǎn),加上中間供應(yīng)商轉(zhuǎn)手的利潤(rùn),運(yùn)費(fèi),等。
例3,HUMIRIA每個(gè)月的價(jià)格,美國(guó)不經(jīng)過(guò)保險(xiǎn)公司折扣的價(jià)格是3430.82 美元,美國(guó)經(jīng)過(guò)保險(xiǎn)公司的折扣后的價(jià)格2504.5美元,全球第二貴的國(guó)家,德國(guó)的價(jià)格是1749.26美元。如果國(guó)內(nèi)采購(gòu)美國(guó)的參比制劑,就要以3430.82美元為起點(diǎn),加上中間供應(yīng)商轉(zhuǎn)手的利潤(rùn),運(yùn)費(fèi),等。
即使打折以后的藥品,美國(guó)病人也不是支付打折以后剩余的全部的價(jià)格的。保險(xiǎn)公司一般讓病人支付一部分的價(jià)格,具體每個(gè)保險(xiǎn)公司不同。但是,像HUMIRIA這樣的藥品,即使支付10%也是無(wú)法承受的,美國(guó)病人又是如何來(lái)對(duì)付天價(jià)的新特藥品呢?這里就不談沒(méi)有保險(xiǎn)的窮人,因?yàn)楦F人患了大病,國(guó)家政府的低保,100%保住的。
我們用HUMIRIA做個(gè)例子,比如,保險(xiǎn)公司支付75%, 剩下25% 美國(guó)病人也是支付不起的。怎么辦? GILEAD公司有一個(gè)病人資助計(jì)劃,經(jīng)過(guò)評(píng)估入選的病人,只需要每個(gè)月支付5美元,如果特別窮的,一分錢也不需要支付。 如果你的收入超過(guò)一定的限額,不符合GILEAD病人資助計(jì)劃的,怎么辦?美國(guó)醫(yī)療保險(xiǎn),包括最差的保險(xiǎn)–奧巴馬醫(yī)療保險(xiǎn),都有一個(gè)條款,就是病人有一個(gè)每年最高的醫(yī)療花費(fèi)金額的限制,比如6500美元一年,或者6%的工資等,超過(guò)這個(gè)限額以外,所有的醫(yī)療費(fèi)用,全部有保險(xiǎn)公司報(bào)銷。這就是美國(guó)藥品超貴,但是,絕大部分美國(guó)人民,還是可以承受的起的原因。(真實(shí)的一般美國(guó)家庭,沒(méi)有什么積蓄的,連幾千美元的存款都拿不出來(lái)的)。
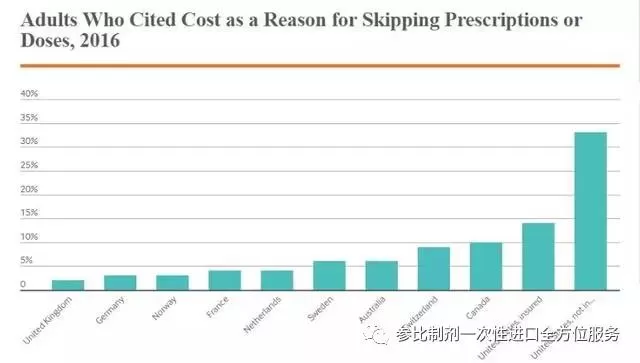
下面的圖表顯示,2016年,美國(guó)有保險(xiǎn)的病人,14%抱怨因?yàn)樗幤穬r(jià)格太高,而停止,或者跳過(guò),或者減少,服用藥品。在沒(méi)有保險(xiǎn)的美國(guó)人中,有33%的病人抱怨因?yàn)樗幤穬r(jià)格太高,而停止,或者跳過(guò),或者減少,服用藥品。這里的停止服用的藥品,包括非救命必須的藥品,很多美國(guó)人服用的藥品,不是100%需要的,跳過(guò)幾次,不一定有什么大的損害的。歐洲國(guó)家,全民醫(yī)保,每次吃藥,只需要支付幾歐元的費(fèi)用,一般只有5%以下的病人抱怨因?yàn)樗幤穬r(jià)格太高,而停止,或者跳過(guò),或者減少,服用藥品。
制藥上市獲批的基礎(chǔ),就是有生物等效性研究證明仿制藥與原研藥在吸收的速率和程度上沒(méi)有顯著差別,所以研發(fā)的基礎(chǔ)就是需要獲得一定數(shù)量的原研產(chǎn)品來(lái)開(kāi)展生物等效性試驗(yàn)。一般情況下,仿制藥公司可以在市場(chǎng)上通過(guò)經(jīng)銷商或批發(fā)商來(lái)購(gòu)買原研制劑。但是,對(duì)于一些安全風(fēng)險(xiǎn)很高的產(chǎn)品,F(xiàn)DA認(rèn)為有必要再加一道“安全門”,避免它們給患者或潛在的使用者帶來(lái)無(wú)法控制的風(fēng)險(xiǎn),那就是REMS。REMS通常要求經(jīng)銷商未經(jīng)許可不得向任何個(gè)體或企業(yè)銷售帶有REMS約束的產(chǎn)品,這就使得仿制藥廠必須向原研藥廠直接購(gòu)買產(chǎn)品。一旦原研藥廠拒絕向仿制藥廠銷售產(chǎn)品,仿制藥公司幾乎沒(méi)有任何合法途徑獲得參比制劑,也就無(wú)法開(kāi)展任何研發(fā)活動(dòng)。這道用以保護(hù)患者的“安全門”,有些聰明的原研藥廠也拿它來(lái)作為規(guī)避競(jìng)爭(zhēng)的“防護(hù)門”。
REMS是什么
2007年FDAAA頒布時(shí)產(chǎn)生了這一新的風(fēng)險(xiǎn)降低計(jì)劃,旨在對(duì)風(fēng)險(xiǎn)極高的產(chǎn)品采取一系列標(biāo)簽以外的措施來(lái)確保處方藥的獲益大于風(fēng)險(xiǎn),不當(dāng)使用帶來(lái)的風(fēng)險(xiǎn)可能包括有極強(qiáng)傳染性的、造成嚴(yán)重過(guò)敏反應(yīng)的、嚴(yán)重肝腎損傷、或者生殖毒性等等。 這些REMS里也經(jīng)常要求ETASU(Elements to Assure Saef Use, 確保安全使用要素),常見(jiàn)的ETASU包括通常包括患者登記、藥師和其他職業(yè)人員需要獲得特殊認(rèn)證才能有配藥資格、對(duì)于醫(yī)生、藥師、或者患者的特殊培訓(xùn)、潛在妊娠婦女服用可能致畸產(chǎn)品前的額外測(cè)試,或者,以及特別的患者監(jiān)控計(jì)劃。
所有的在REMS下的NDA和BLA都必須在提交產(chǎn)品申請(qǐng)的時(shí)候同步遞交一份執(zhí)行REMS計(jì)劃的詳細(xì)時(shí)間表,NDA和BLA產(chǎn)品的REMS計(jì)劃應(yīng)包含額外的特殊用藥指南或患者說(shuō)明書(shū)、與患者和執(zhí)業(yè)人員的交流計(jì)劃、ETASU、執(zhí)行系統(tǒng)等。目前法律要求仿制藥的REMS需要與原研產(chǎn)品一致,與原研企業(yè)達(dá)成一致的“共享REMS計(jì)劃”,事實(shí)上由于涉及到復(fù)雜的法律責(zé)任承擔(dān)問(wèn)題,僅僅是達(dá)成這樣的協(xié)議本身就需要很長(zhǎng)時(shí)間的談判。FDA已經(jīng)意識(shí)到了共享REMS可能會(huì)在操作上形成拖延仿制藥進(jìn)入市場(chǎng)的情況,局長(zhǎng)Gottlieb在2017年11月發(fā)布《對(duì)共享系統(tǒng) REMS 提交使用藥物主文件(DMF)》指南草案的講話中也表示,F(xiàn)DA正在考慮允許仿制藥申請(qǐng)人請(qǐng)求免除與創(chuàng)新藥公司使用共享REMS的要求。【FDA 采取基礎(chǔ)步驟改善仿制藥企業(yè)對(duì)品牌藥樣品的獲取 2017-11-09】
仿制藥廠起訴原研藥廠均以和解收尾
由于REMS體系是從2007年FDAAA頒布時(shí)才開(kāi)始出現(xiàn)的,而且設(shè)計(jì)REMS規(guī)定的大品種數(shù)量有限,所以到目前為止,在獲取參比制劑的問(wèn)題上打官司的案件只有7起,其中最著名的就是Celgene的沙利度胺(反應(yīng)停)。 由于沙利度胺有可能導(dǎo)致嚴(yán)重的胎兒致畸,1998年FDA批準(zhǔn)時(shí)就嚴(yán)格限制了該產(chǎn)品的流通渠道(當(dāng)時(shí)還沒(méi)有REMS體系,之一計(jì)劃被稱為STEPS,System for Thalidomide Education and Prescribing Safety),STEPS也限制了仿制藥公司從其他渠道獲取參比制劑,2008年Lannet公司嘗試從Celgene購(gòu)買參比制劑失敗后將它告上法庭,起訴Celgene濫用安全限制要求來(lái)阻礙仿制藥廠獲取參比制劑,以強(qiáng)迫消費(fèi)者支付壟斷的高昂價(jià)格,Celgene反訴被駁回后不久,案子就以雙方和解結(jié)束。
同樣因?yàn)闊o(wú)法獲得樣品起訴原研公司的還有2013年Actelion為波生坦訴Apotex,2014年Mylan為雷利米得訴Celgene,2014年多家企業(yè)為舒倍生訴Reckitt,2015年Natco為安倍生坦訴Gilead,2015年多家企業(yè)為沙利度胺和雷利米得訴Celgene,2017年Amneal為復(fù)方舒倍生訴Indivior(前身為Reckitt)。 所有已經(jīng)結(jié)束的案例,不論是否涉及仿制藥和原研藥的共享REMS協(xié)議,最終都以和解告終,沒(méi)有形成產(chǎn)生允許仿制藥獲取參比制劑的法律通道。
建議立法保障仿制藥企獲取參比制劑
和FDA一樣,對(duì)于原研藥公司利用REMS阻攔仿制藥廠獲取參比制劑的情況,國(guó)會(huì)的進(jìn)展也是“雷聲大雨點(diǎn)小”。兩黨議員都對(duì)這個(gè)問(wèn)題表示了關(guān)注而且提出了兩部建議的法案:FAST法案(Fair Access for Safe and Timely Generics Act of 2015)和CREATS法案(Creating and Restoring Equal Access To Equivalent Samples Act of 2017)。它們分別是由俄亥俄州共和黨議員Stiver Steve和佛蒙特州民主黨議員Laehy Patrick Joseph在2015年和2017年提出的。但是這兩部建議法案自從提交到現(xiàn)在暫時(shí)還沒(méi)有被國(guó)會(huì)考慮,仍處在法案推介階段。
這兩份法案都試圖從立法的角度維護(hù)Hatch-Waxman法案的精神,把仿制藥競(jìng)爭(zhēng)作為降低藥品開(kāi)支,惠及民眾的辦法之一。 兩部建議的法案都提到了要求原研藥廠在FDA批準(zhǔn)的情況下,在仿制藥廠提出請(qǐng)求的一定時(shí)間內(nèi)提供帶有REMS要求的樣品,同時(shí)也增加了更多有關(guān)生物等效性試驗(yàn)中出現(xiàn)安全問(wèn)題的法律責(zé)任分配問(wèn)題。
FDA前副局長(zhǎng)實(shí)名反對(duì),新法案爭(zhēng)議紛紛
這兩部法案在國(guó)會(huì)沒(méi)有繼續(xù)推動(dòng)的跡象,反而引來(lái)了批評(píng)聲音,F(xiàn)DA前副局長(zhǎng)Peter Pitts在著名的《投資人商報(bào)》上發(fā)表評(píng)論文章,聲稱如果允許仿制藥公司獲取REMS會(huì)嚴(yán)重影響患者的安全,會(huì)摧毀FDA盡力為安全用藥搭建的最后屏障,而且會(huì)讓原研藥公司承擔(dān)不必要的法律責(zé)任。
而著名的Lachman公司的FDA前官員Bob Pollock先生則發(fā)文直指這位前局長(zhǎng)說(shuō)話不合事實(shí)和邏輯混淆,首先生物等效性試驗(yàn)的對(duì)象絕大多數(shù)是健康志愿者而非患者,其次,生物等效性試驗(yàn)的方案是經(jīng)過(guò)FDA批準(zhǔn)的,包含在REMS(或者共享REMS)下的執(zhí)行方案,最后,生物等效性試驗(yàn)的樣本數(shù)較少,樣品嚴(yán)格控制,不會(huì)引入大量市場(chǎng)上需要服藥的患者。唯一的爭(zhēng)議在于,由于生物等效性試驗(yàn)通常由CRO公司開(kāi)展,不直接受原研藥公司監(jiān)控 , 一旦出現(xiàn)安全性問(wèn)題應(yīng)如何分配法律責(zé)任。Pollock先生認(rèn)為這類批評(píng)是“風(fēng)馬牛不相及”的批評(píng) , 而且患者由于壟斷高昂價(jià)格買不到藥比大公司承擔(dān)法律責(zé)任是更重要的公共健康問(wèn)題。
多次聽(tīng)證已經(jīng)讓我們知道由于這種競(jìng)爭(zhēng)壁壘帶來(lái)的藥價(jià)提升可能在幾十倍的數(shù)量級(jí)上 , 我們不知道這位前副局長(zhǎng)是揣著明白裝糊涂,還是真有對(duì)新建議立法的擔(dān)憂,但是可以看出的是,這樣的言論 , 無(wú)疑是對(duì)原研藥公司有利的。
問(wèn)題到底有多嚴(yán)重?
看到這里您可能會(huì)問(wèn),那到底有多少產(chǎn)品會(huì)受影響?答案可能不如我們想象的多。截止到2018年4月FDA公布的所有已獲批REMS涉及66個(gè)物質(zhì)78個(gè)產(chǎn)品,其中10個(gè)共享REMS計(jì)劃,10個(gè)ANDA,13個(gè)BLA和45個(gè)NDA。 這些REMS產(chǎn)品大部分是激素類或神經(jīng)抑制產(chǎn)品 , 還有一些涉及到使用器械的復(fù)雜組合產(chǎn)品。 當(dāng)然 , 也都是利潤(rùn)頗豐的品種。 隨著越來(lái)越多企業(yè)自主提交REMS計(jì)劃和用藥指南補(bǔ)充說(shuō)明 , 可以預(yù)見(jiàn)的是,使用REMS可能會(huì)成為原研藥企業(yè)對(duì)抗仿制藥競(jìng)爭(zhēng)的又一有力工具。但最后,不論是原研企業(yè)繼續(xù)壟斷還是巨額賠償?shù)耐ネ夂徒猓袚?dān)成本的還是患者和支付方。
]]>

生物制藥市場(chǎng)火火火
據(jù)IMS Health統(tǒng)計(jì),2014年全球生物制藥市場(chǎng)規(guī)模已達(dá)到2140億美金,市場(chǎng)占有份額也從2001年的10.5%增長(zhǎng)至2014年的21.3%,以高于全球制藥市場(chǎng)增長(zhǎng)的良好態(tài)勢(shì)蓬勃發(fā)展。近幾年來(lái),技術(shù)方面的突破也會(huì)加速生物技術(shù)在制藥領(lǐng)域的應(yīng)用和新藥的研發(fā)。在這樣的背景下,全球制藥巨頭都瞄準(zhǔn)了生物制藥這一新興的領(lǐng)域,爭(zhēng)相開(kāi)發(fā)生物醫(yī)藥市場(chǎng)。
美國(guó)、德國(guó)和日本位列生物制藥市場(chǎng)占有前三的排名,其中具備絕對(duì)優(yōu)勢(shì)的美國(guó),市場(chǎng)份額從2010年的45.4%增至2014年的49.4%。此外,中國(guó)的生物制藥發(fā)展勢(shì)頭喜人,市場(chǎng)份額從2010年的1.7%增長(zhǎng)至2014年的2.8%。
全球主要國(guó)家生物藥市場(chǎng)份額一覽
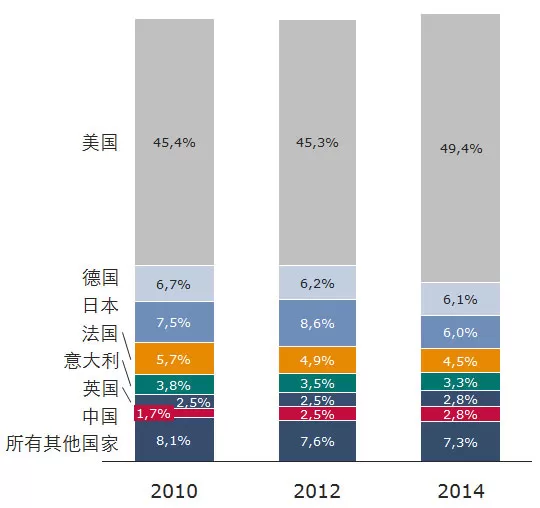
來(lái)源: IMS Health
從疾病領(lǐng)域的市場(chǎng)占有率看,排名前五的生物制劑治療領(lǐng)域依次為:類風(fēng)濕性關(guān)節(jié)炎(18%)、糖尿病(17%)、腫瘤(13%),以及疫苗和免疫激動(dòng)劑(占比分別為7%和6%)。
3月28日,在由中共廣州市委、廣州市人民政府主辦,廣藥醫(yī)藥集團(tuán)有限公司承辦的“2017中國(guó)廣州國(guó)際投資年會(huì)生物醫(yī)藥健康產(chǎn)業(yè)分論壇”上,廣州白云山南方抗腫瘤生物制品股份有限公司成立揭牌儀式,并明確該公司將主要開(kāi)展新型抗腫瘤疫苗的開(kāi)發(fā)及應(yīng)用項(xiàng)目,產(chǎn)品有望填補(bǔ)國(guó)內(nèi)治療性肝癌疫苗的空白。
由此可以看到,廣藥白云山在生物制藥制劑領(lǐng)域正是選擇了以疾病市場(chǎng)占有率前五的疫苗為切入。
合作開(kāi)發(fā),新型抗腫瘤疫苗為全球首創(chuàng)
新康界了解到,廣州白云山南方抗腫瘤生物制品股份有限公司是廣藥白云山屬下全資子公司廣州白云山拜迪生物醫(yī)藥有限公司與南方醫(yī)科大學(xué)南方醫(yī)院、東莞市長(zhǎng)大生物科技有限公司、廣東省粵科財(cái)政股權(quán)投資有限公司及李明松五方共同發(fā)起成立,主要承擔(dān)的抗腫瘤疫苗項(xiàng)目,注冊(cè)資本為人民幣9
]]>春節(jié)前,從全國(guó)食品藥品醫(yī)療器械檢驗(yàn)工作電視電話會(huì)議上傳出消息,2017年仿制藥一致性評(píng)價(jià)工作將由啟動(dòng)、籌備階段轉(zhuǎn)入品種申報(bào)、檢查檢驗(yàn)和審評(píng)的全面實(shí)施階段。事實(shí)上,到1月20日止,國(guó)家食品藥品監(jiān)管總局(CFDA)已結(jié)束了對(duì)一致性評(píng)價(jià)研究現(xiàn)場(chǎng)核查、生產(chǎn)現(xiàn)場(chǎng)檢查、臨床試驗(yàn)核查、有因檢查等指導(dǎo)原則的意見(jiàn)征求。
在2016年工作的基礎(chǔ)上,CFDA將繼續(xù)推進(jìn)參比制劑備案、技術(shù)指導(dǎo)原則的完善、申報(bào)資料的規(guī)范、復(fù)核檢驗(yàn)?zāi)0宓闹贫ǖ葮I(yè)務(wù)工作。目前,289個(gè)品種的復(fù)檢工作和復(fù)核指南均已分配到31個(gè)省藥檢所,每個(gè)品種都有專屬技術(shù)標(biāo)準(zhǔn)和復(fù)檢機(jī)構(gòu)。各承擔(dān)檢驗(yàn)工作的機(jī)構(gòu)將對(duì)生產(chǎn)企業(yè)報(bào)送的一致性評(píng)價(jià)資料進(jìn)行復(fù)核,根據(jù)復(fù)核結(jié)果,逐步建立我國(guó)的口服固體制劑溶出曲線數(shù)據(jù)庫(kù)。
2017年,仿制藥一致性評(píng)價(jià)將全面推進(jìn)。然而相當(dāng)一部分的制藥企業(yè)受制于高昂的評(píng)價(jià)費(fèi)用,面臨著逐步退出或放棄部分品種的選擇。大家不禁會(huì)提出一系列的疑問(wèn):“企業(yè)該如何選品種?低價(jià)藥、小品種怎么做?對(duì)未來(lái)行業(yè)格局有什么影響?”帶著這些問(wèn)題,眾多醫(yī)藥大咖齊聚一堂在米交匯上展開(kāi)了激烈的討論。
點(diǎn)評(píng)專家 朱迅
原白求恩醫(yī)科大學(xué)副校長(zhǎng)、新天域資本顧問(wèn)、《藥學(xué)進(jìn)展》副主編
一致性評(píng)價(jià)曾走過(guò)血淋淋的歷史,美國(guó)搞過(guò),日本也搞過(guò),中國(guó)現(xiàn)在已經(jīng)是世界第二大醫(yī)藥國(guó),其經(jīng)濟(jì)總量也已排在世界第二。作為政府,要讓每一個(gè)公民能用上放心的藥品。作為行業(yè),每個(gè)企業(yè)自身,無(wú)論是生產(chǎn)企業(yè)也包括研發(fā)企業(yè),也包括很多CRO公司,應(yīng)該對(duì)得起我們從事的職業(yè),使安全可靠有效的藥品變成老百姓服用的放心藥。
歐陽(yáng)靜波:新規(guī)引發(fā)行業(yè)大洗牌
廣西梧州中恒集團(tuán)總裁 歐陽(yáng)靜波
從一系列藥監(jiān)新政來(lái)看,這是新常態(tài)帶給我們產(chǎn)業(yè)調(diào)整的必然。一致性評(píng)價(jià)在國(guó)外同樣經(jīng)歷過(guò)痛苦的過(guò)程,美國(guó)、日本都是如此,他們現(xiàn)在已經(jīng)走到了世界前列。最早期的一致性評(píng)價(jià)幾十萬(wàn)一百萬(wàn),現(xiàn)在價(jià)碼是300萬(wàn)-500萬(wàn),甚至達(dá)到600萬(wàn),對(duì)于生產(chǎn)企業(yè)來(lái)說(shuō)覺(jué)得不可接受,但這確確實(shí)實(shí)是我們國(guó)家藥政和時(shí)代的進(jìn)步。
一致性評(píng)價(jià)新規(guī)出來(lái)之后,做化藥仿制藥的公司感覺(jué)到了比較大的壓力,大家感覺(jué)到這一輪供給側(cè)改革確確實(shí)實(shí)要淘汰落后產(chǎn)能,會(huì)有大的洗牌。在這個(gè)過(guò)程中,會(huì)給輔料企業(yè)和CRO企業(yè)帶來(lái)機(jī)會(huì)。
一致性評(píng)價(jià)讓制藥工業(yè)企業(yè)重新進(jìn)行產(chǎn)品篩選和中心定位,往往壓力才是動(dòng)力,沒(méi)有急迫性,沒(méi)有背水一戰(zhàn)的決心,一個(gè)企業(yè)不會(huì)置之死地而后生,重新定位產(chǎn)品篩選,這也是一種機(jī)遇。資本與并購(gòu),包括海外和國(guó)內(nèi)的并購(gòu),也會(huì)給我們的產(chǎn)品線補(bǔ)充帶來(lái)機(jī)會(huì)。
一致性評(píng)價(jià)帶來(lái)的挑戰(zhàn)非常大,壓力非常大,但我個(gè)人更多的感受是時(shí)代發(fā)展,因?yàn)樗菚r(shí)代發(fā)展的脈搏,前進(jìn)的動(dòng)力,所以我們看到更多的是機(jī)遇。
點(diǎn)評(píng):進(jìn)步一定伴隨著淘汰落后,過(guò)程就是洗牌,意味著倒出來(lái)很多空間,也出現(xiàn)了很多機(jī)會(huì),總結(jié)得很精辟。
陳永紅:升級(jí)企業(yè)的質(zhì)量、體系、生產(chǎn)
廣東眾生藥業(yè)董事總經(jīng)理 陳永紅
在國(guó)家公布的289個(gè)制藥產(chǎn)品中,廣東眾生藥業(yè)的品種數(shù)量排名第八位,我們非常主動(dòng)地參與仿制藥的一致性評(píng)價(jià),形成了一些溝通機(jī)制。到底做哪些產(chǎn)品,不做哪些產(chǎn)品,我們有產(chǎn)品篩選模型,每個(gè)月有一次項(xiàng)目進(jìn)度匯報(bào)會(huì)。我們希望借此機(jī)會(huì)做三個(gè)升級(jí):質(zhì)量、體系、生產(chǎn)升級(jí)。這兩年我們花大力氣做生產(chǎn)研究,如果沒(méi)有生產(chǎn)的管理,前期的研發(fā)無(wú)法產(chǎn)業(yè)化,未來(lái)也沒(méi)有競(jìng)爭(zhēng)力,這就是我們做決策的邏輯。
點(diǎn)評(píng):陳總講的是蘊(yùn)含很深的決策考量。品種多的面臨篩選,品種少的也在想辦法,在洗牌的過(guò)程中怎么抓住機(jī)會(huì)。如何經(jīng)營(yíng)選擇,每個(gè)企業(yè)有每個(gè)企業(yè)自己不同的選擇邏輯,但是過(guò)程中還有很多主觀因素需要思考。
劉平:生物等效是洗牌的過(guò)程
深圳奧薩醫(yī)藥研發(fā)總裁 劉平
我們基本上不做仿制藥,在技術(shù)上談點(diǎn)體會(huì)。最近我們從另外一個(gè)側(cè)面研討,如果沒(méi)辦法驗(yàn)證生物等效怎么辦?臨床等效怎么做?國(guó)外有什么例子,我們做了一點(diǎn)這方面的探討。
我們看到國(guó)外有很多這方面的例子,生物等效沒(méi)法做,比如天然人體存在的成分,或者生物做出來(lái)就是不等效,這種情況下又認(rèn)為這個(gè)藥品是必須的,怎么辦?就要用臨床等效,臨床等效時(shí)間長(zhǎng),費(fèi)用高,現(xiàn)在看來(lái)好多情況不一定。從科學(xué)角度講,臨床等效肯定高于生物等效。
當(dāng)你生物等效無(wú)法做,或者說(shuō)生物本身不等效時(shí),這種情況下國(guó)外有成功的例子,可以供大家參考。
生物等效是洗牌的過(guò)程,也給了真正的仿制藥未來(lái)有重新定價(jià)的機(jī)會(huì),與原研藥形成差不多的價(jià)格,在一個(gè)價(jià)格水平上競(jìng)爭(zhēng)。
點(diǎn)評(píng):在洗牌的過(guò)程中,一些創(chuàng)新企業(yè)正好可以借助此次機(jī)會(huì)進(jìn)入仿制藥市場(chǎng)。我們做過(guò)一次調(diào)研,感覺(jué)到企業(yè)對(duì)一致性評(píng)價(jià)的理解偏差非常大,很多企業(yè)根本沒(méi)有想到一致性評(píng)價(jià)對(duì)產(chǎn)業(yè)格局的真正影響是什么,真正影響絕對(duì)不僅限于現(xiàn)在這289個(gè)基藥品種,要看得更長(zhǎng)遠(yuǎn)一些。
黃凌云:對(duì)企業(yè)來(lái)說(shuō)是機(jī)會(huì)
廣東瑞興醫(yī)藥董事長(zhǎng) 黃凌云
廣東瑞興醫(yī)藥2016年1月份上新三板,以商業(yè)為主、研發(fā)生產(chǎn)為輔。一致性評(píng)價(jià)對(duì)于我們這類企業(yè)來(lái)說(shuō)無(wú)疑是機(jī)會(huì)。我們接觸的上游企業(yè)都是中小藥廠,一致性評(píng)價(jià)涵蓋了這么多產(chǎn)品,給了很多機(jī)會(huì)。我們接下來(lái)2-3年干的就是這個(gè)事,找兩三個(gè)新的合作伙伴,拿些一致性評(píng)價(jià)的品種回來(lái)做,不僅要盯著289個(gè)基藥品種,后面還將有更多的產(chǎn)品。
點(diǎn)評(píng):大家千萬(wàn)別把一致性評(píng)價(jià)作為孤立的事件來(lái)看待,緊接著,還會(huì)有生產(chǎn)工藝核查,比一致性評(píng)價(jià)的影響還要深。這個(gè)過(guò)程將逼著企業(yè)一步步向規(guī)范、可控、科學(xué)、嚴(yán)謹(jǐn)靠攏。
黃慶文:壓力很大,但要迎難而上
廣東逸舒制藥董事長(zhǎng) 黃慶文
逸舒制藥共有兩家藥廠,一致性評(píng)價(jià)涉及八個(gè)品種。對(duì)中小藥企來(lái)講,我們覺(jué)得壓力很大,但肯定要迎難而上。在品種選擇上,先行選擇銷售額較大的兩三個(gè)品種來(lái)做,最后爭(zhēng)取做到五六個(gè)。
我們希望通過(guò)努力能有1-2個(gè)品種沖到前三家之內(nèi),從銷售的角度看,進(jìn)入前三家,在招標(biāo)上有很大的優(yōu)勢(shì)。國(guó)內(nèi)一開(kāi)始搞GMP的時(shí)候,很多人拖著,結(jié)果前期通過(guò)GMP的企業(yè)搶占了先機(jī)。
我們現(xiàn)在也在收購(gòu)一些品種,一致性評(píng)價(jià)后,收購(gòu)的策略發(fā)生了一定變化,比如我們可能更偏向于中藥品種。
點(diǎn)評(píng):這次一定是剩者為王,想剩下來(lái)就要知道哪有坑、哪有陷阱、哪是思路。企業(yè)可能有很多死法,有擠死、餓死、撐死,一致性評(píng)價(jià)給了很好的機(jī)會(huì),每個(gè)企業(yè)都應(yīng)該圍繞自己的情況做幾輪深入的探討。
張明:一致性評(píng)價(jià)提高仿制藥質(zhì)量
北京星昊醫(yī)藥研發(fā)副總 張明
國(guó)產(chǎn)的仿制藥質(zhì)量和療效不能跟原研藥等同,所以價(jià)格和市場(chǎng)占有率就不能與原研藥等同。這是經(jīng)濟(jì)問(wèn)題還是政策問(wèn)題,抑或是技術(shù)問(wèn)題?如果是經(jīng)濟(jì)問(wèn)題,用技術(shù)手段能不能解決?國(guó)產(chǎn)藥不如進(jìn)口藥,在很大程度上,價(jià)格水平是決定因素。如果在價(jià)格上有空間,國(guó)產(chǎn)藥都愿意做好,也能夠做好。
國(guó)內(nèi)醫(yī)藥市場(chǎng)充斥著大量療效不確切、缺少循證醫(yī)學(xué)依據(jù)的品種,這些品種利用率很高,占用了大量醫(yī)療資源。建議采取一些手段,讓療效不確切的品種退出市場(chǎng)。一致性評(píng)價(jià)首先選擇289個(gè)基藥“開(kāi)刀”,回避了那些“有問(wèn)題”的品種,這樣一來(lái),有可能使價(jià)廉效佳的品種受到限制,而一些不好的藥有了生存空間。
對(duì)于找不到參比制劑的品種,由企業(yè)開(kāi)展臨床實(shí)驗(yàn)。如果沒(méi)有一家開(kāi)展臨床實(shí)驗(yàn),會(huì)不會(huì)出現(xiàn)一個(gè)情況?市場(chǎng)上這個(gè)產(chǎn)品仍在售,盡管它是無(wú)效的。
從好的方面講,一致性評(píng)價(jià)能夠促進(jìn)行業(yè)重組,對(duì)市場(chǎng)重新洗牌,加速與國(guó)際接軌,如果能實(shí)現(xiàn)這個(gè)目標(biāo),一致性評(píng)價(jià)對(duì)于仿制藥的質(zhì)量提高將起到很大的作用。這需要國(guó)家有強(qiáng)大的決心、人員、政策配套,如果不能執(zhí)行下去,可能會(huì)出現(xiàn)管住一塊、另一塊仍然亂象重生的現(xiàn)象。
點(diǎn)評(píng):一致性評(píng)價(jià)必須先從基藥開(kāi)刀,基藥的處方涉及到每個(gè)人,路要一步步走,做完固體制劑的一致性評(píng)價(jià)之后,一定是生化藥,也包括中藥制劑。在一定程度上,國(guó)家監(jiān)管部門首先考慮的是用藥安全,藥物評(píng)價(jià)安全、有效、可控是全球統(tǒng)一的標(biāo)準(zhǔn)。
一致性評(píng)價(jià)牽動(dòng)很多,但是大格局不會(huì)變,就是要做到讓大家吃的藥是安全、可控、有良心的藥。
江鴻:做中國(guó)的仿制藥領(lǐng)先企業(yè)
江西施美藥業(yè)董事長(zhǎng) 江鴻
我們一直在講創(chuàng)新藥,但實(shí)際上創(chuàng)新藥不好做。我建議還是先做好仿制藥,我的企業(yè)定位就是做中國(guó)的仿制藥領(lǐng)先企業(yè),如果還往高走,就做中國(guó)的改良型藥品領(lǐng)先企業(yè)。
魏林華:市場(chǎng)容量未來(lái)會(huì)擴(kuò)大
廣東三信藥業(yè)董事長(zhǎng) 魏林華
我們?cè)瓉?lái)是以代理經(jīng)銷為主的企業(yè),也兼一些項(xiàng)目的投資運(yùn)營(yíng),我們也想抓住一致性評(píng)價(jià)這樣的機(jī)會(huì),投資一些產(chǎn)品。但這個(gè)挑戰(zhàn)不小。一致性評(píng)價(jià)對(duì)于行業(yè)競(jìng)爭(zhēng)度的提高肯定有幫助,對(duì)有經(jīng)驗(yàn)的人,一致性評(píng)價(jià)對(duì)他們是很有利的。對(duì)中小企業(yè)也有很多機(jī)會(huì),市場(chǎng)容量以后會(huì)擴(kuò)大。
做一致性評(píng)價(jià)這么難,低價(jià)藥小品種花一兩千萬(wàn)去做恐怕也不大現(xiàn)實(shí),這類品種怎么做?我把這個(gè)問(wèn)題拋出來(lái)。
點(diǎn)評(píng):你困惑,所有企業(yè)都困惑,我也很困惑。但你認(rèn)為中國(guó)需要5000家制藥企業(yè)嗎?或許,誰(shuí)能夠盡早地不困惑,誰(shuí)就走在了前面。
張自然:選品種是一項(xiàng)挑戰(zhàn)
中投中財(cái)投資公司執(zhí)行董事、中國(guó)中藥協(xié)會(huì)副會(huì)長(zhǎng) 張自然
企業(yè)怎么選品種? 289個(gè)品種對(duì)應(yīng)的17440個(gè)批文,其中有一個(gè)批文的是400多個(gè)廠家。企業(yè)怎么選,這是很大的挑戰(zhàn)。粗略算來(lái),現(xiàn)在全國(guó)過(guò)億品種大大小小差不多有1500個(gè)。一致性評(píng)價(jià)肯定是為了療效確切,又要安全,淘汰落后產(chǎn)能的方式很多,現(xiàn)在GMP已經(jīng)過(guò)去了,也沒(méi)有覺(jué)得藥廠死了多少,盡管品種的質(zhì)量有待考察,最終還是要提高行業(yè)的集中度,淘汰產(chǎn)能。
現(xiàn)在制藥企業(yè)本身作為主體,重點(diǎn)就是品種選擇的策略,以帶動(dòng)延伸的CRO優(yōu)質(zhì)輔料、優(yōu)質(zhì)原料等。
]]>
附人體生物等效性試驗(yàn)豁免指導(dǎo)原則的通告(2016年第87號(hào))
本指導(dǎo)原則適用于仿制藥質(zhì)量和療效一致性評(píng)價(jià)中口服固體常釋制劑申請(qǐng)生物等效性(Bioequivalence)豁免。該指導(dǎo)原則是基于國(guó)際公認(rèn)的生物藥劑學(xué)分類系統(tǒng)(Biopharmaceutics Classification System,以下簡(jiǎn)稱BCS)起草。
一、藥物BCS分類
BCS系統(tǒng)是按照藥物的水溶性和腸道滲透性對(duì)其進(jìn)行分類的一個(gè)科學(xué)架構(gòu)。當(dāng)涉及到口服固體常釋制劑中活性藥物成分(Active Pharmaceutical Ingredient,以下簡(jiǎn)稱API)在體內(nèi)吸收速度和程度時(shí),BCS系統(tǒng)主要考慮以下三個(gè)關(guān)鍵因素,即:藥物溶解性(Solubility)、腸道滲透性(Intestinal permeability)和制劑溶出度(Dissolution)。
(一)溶解性
溶解性分類根據(jù)申請(qǐng)生物等效豁免制劑的最高劑量而界定。當(dāng)單次給藥的最高劑量對(duì)應(yīng)的API在體積為250ml(或更少)、pH值在1.0-6.8范圍內(nèi)的水溶性介質(zhì)中完全溶解,則可認(rèn)為該藥物為高溶解性。250ml的量來(lái)源于標(biāo)準(zhǔn)的生物等效性研究中受試者用于服藥的一杯水的量。
(二)滲透性
滲透性分類與API在人體內(nèi)的吸收程度間接相關(guān)(指吸收劑量的分?jǐn)?shù),而不是全身的生物利用度),與API在人體腸道膜間質(zhì)量轉(zhuǎn)移速率直接相關(guān),或者也可以考慮其他可以用來(lái)預(yù)測(cè)藥物在體內(nèi)吸收程度的非人體系統(tǒng)(如使用原位動(dòng)物、體外上皮細(xì)胞培養(yǎng)等方法)對(duì)滲透性進(jìn)行分類。當(dāng)一個(gè)口服藥物采用質(zhì)量平衡測(cè)定的結(jié)果或是相對(duì)于靜脈注射的參照劑量,顯示在體內(nèi)的吸收程度≥85%以上(并且有證據(jù)證明藥物在胃腸道穩(wěn)定性良好),則可說(shuō)明該藥物具有高滲透性。
(三)溶出度
口服固體常釋制劑具有快速溶出的定義是:采用中國(guó)藥典2015版附錄通則(0931)方法1 (籃法),轉(zhuǎn)速為每分鐘100轉(zhuǎn),或是方法2(槳法),轉(zhuǎn)速為每分鐘50或75轉(zhuǎn),溶出介質(zhì)體積為500ml(或更少),在溶出介質(zhì):(1) 0.1mol/L HCl或是不含酶的模擬胃液;(2)pH4.5緩沖介質(zhì);(3)pH6.8緩沖介質(zhì)或是不含酶的模擬腸液中,30分鐘內(nèi)API的溶出均能達(dá)到標(biāo)示量的85%以上。
口服固體常釋制劑具有非常快速溶出的定義是:在上述條件下15分鐘內(nèi)API的溶出均能達(dá)到標(biāo)示量的85%以上。
根據(jù)BCS分類系統(tǒng),藥品被分為以下四類:
第一類:高溶解性、高滲透性(High Solubility- High Permeability)
第二類:低溶解性、高滲透性(Low Solubility-High Permeability)
第三類:高溶解性、低滲透性(High Solubility-Low Permeability)
第四類:低溶解性、低滲透性(Low Solubility-Low Permeability)
當(dāng)口服固體常釋制劑在體內(nèi)的溶出相對(duì)于胃排空時(shí)間快或非常快,并且具有很高的溶解度時(shí),藥物的吸收速率和吸收程度就不會(huì)依賴于藥物的溶出時(shí)間或在胃腸道的通過(guò)時(shí)間。因此,在這種情況下,對(duì)于BCS分類1類和3類的藥物,只要處方中的其他輔料成分不顯著影響API的吸收,則不必證明該藥物在體內(nèi)生物利用度和生物等效的可能性,即生物等效性豁免。
二、基于BCS的生物等效豁免
(一)對(duì)于BCS 1類的藥物需要證明以下幾點(diǎn):
1.藥物具有高溶解性;
2.藥物具有高滲透性;
3.仿制和參比制劑均為快速溶出,并且制劑中不含有影響主藥成分吸收速率和吸收程度的任何輔料。
(二)對(duì)于BCS 3類的藥物需要證明以下幾點(diǎn):
1.藥物具有高溶解性;
2.仿制和參比制劑均具有非常快速的溶出;
3.仿制制劑和參比制劑應(yīng)處方完全相同,各組成用量相似,當(dāng)放大生產(chǎn)和上市后變更時(shí),制劑處方也應(yīng)完全相同。對(duì)于上市后變更的有關(guān)要求參見(jiàn)《已上市化學(xué)藥品變更研究的技術(shù)指導(dǎo)原則(一)》相關(guān)內(nèi)容。
(三)對(duì)于處方相同,活性成分及輔料成相似比例的不同規(guī)格同種樣品,通常高劑量規(guī)格已做過(guò)BE試驗(yàn)的,低劑量規(guī)格可申請(qǐng)免做BE試驗(yàn),有些品種由于安全性等原因,可選擇較低劑量規(guī)格進(jìn)行體內(nèi)生物等效性試驗(yàn),不同品種有所差異,具體選擇要求參見(jiàn)《以藥動(dòng)學(xué)參數(shù)為終點(diǎn)評(píng)價(jià)指標(biāo)的化學(xué)藥物仿制藥人體生物等效性研究技術(shù)指導(dǎo)原則》相關(guān)內(nèi)容。
(四)生物等效豁免申請(qǐng)的其他影響因素
當(dāng)一個(gè)口服固體常釋制劑申請(qǐng)基于BCS分類的生物等效性豁免時(shí),應(yīng)注意以下因素可能影響生物等效豁免:
1.輔料
BCS1類藥物:輔料有時(shí)候可能會(huì)影響藥物的吸收速率和吸收程度。一般來(lái)說(shuō)使用國(guó)家食品藥品監(jiān)督管理總局已經(jīng)批準(zhǔn)的常釋制劑常用輔料,對(duì)于BCS1類快速溶出的常釋制劑的藥物吸收速率和吸收程度不會(huì)有影響。為了支持生物等效豁免,常釋制劑中輔料的用量應(yīng)該和該輔料在處方中對(duì)應(yīng)的功能保持一致(比如潤(rùn)滑劑)。
當(dāng)使用新的輔料,或者非常規(guī)的大量使用常釋制劑常用輔料,要補(bǔ)充提交該輔料的使用沒(méi)有影響制劑生物利用度的證明資料。可以通過(guò)將簡(jiǎn)單的水溶液作為參比制劑來(lái)開(kāi)展生物利用度研究。大量使用特定的輔料,例如表面活性劑(如聚山梨醇酯80)和甜味劑(如甘露醇或山梨醇),可能會(huì)有問(wèn)題。
BCS3類藥物:該類藥物和BCS1類藥物不同,如果想要申請(qǐng)生物等效豁免,必須有更充分的科學(xué)依據(jù)。BCS3類藥物制劑必須與參比制劑含有相同的輔料組成。這主要是考慮輔料可能對(duì)低滲透性藥物的吸收影響更顯著。因此,仿制制劑的輔料種類必須與參比制劑完全相同,輔料的用量應(yīng)與參比制劑相似或相同。
2.前藥(Prodrugs)
前藥的滲透性通常取決于轉(zhuǎn)化藥物的機(jī)理和(解剖學(xué)上的)部位。若藥物前體-藥物的轉(zhuǎn)化主要表現(xiàn)在腸道膜滲透之后,則應(yīng)測(cè)定該藥物前體的滲透性。若轉(zhuǎn)化表現(xiàn)在腸道膜滲透之前,則應(yīng)測(cè)定該藥物的滲透性。藥物前體和藥物的溶出、pH溶解度數(shù)據(jù)也應(yīng)與之相關(guān)。
3.復(fù)方制劑
當(dāng)口服固體常釋的復(fù)方制劑中各活性組分均為BCS1類藥物,可按BCS1類藥物要求申請(qǐng)生物豁免,但應(yīng)證明各組分之間以及各組分與所有輔料之間沒(méi)有藥物代謝動(dòng)力學(xué)相互作用,否則不能申請(qǐng)豁免。當(dāng)口服固體常釋的復(fù)方制劑中各組分均為BCS3類藥物或有BCS1類和BCS3藥物,應(yīng)按BCS3類藥物要求申請(qǐng)生物豁免,除證明各組分之間無(wú)藥物代謝動(dòng)力學(xué)相互作用外,還應(yīng)證明所有輔料為國(guó)家食品藥品監(jiān)督管理總局已經(jīng)批準(zhǔn)的常釋制劑常用輔料。
4.基于BCS 的生物豁免對(duì)下列情況不適用:
(1)治療范圍狹窄的藥品
受治療藥物濃度或藥效監(jiān)控的制約,按狹窄的治療范圍設(shè)計(jì)的制劑,不適用生物等效性豁免。如:地高辛、鋰制劑、苯妥英、茶堿和華法林阻凝劑。
(2)口腔吸收制劑
由于BCS分類是基于胃腸粘膜的滲透和吸收,因此不適用于口腔吸收制劑,如:類似舌下片或頰下片的制劑。對(duì)于口含片、口腔崩解片等,如果該制劑從口腔吸收也不適用。
三、申請(qǐng)生物等效豁免應(yīng)提供的資料
(一)高溶解性的數(shù)據(jù)支持(或文獻(xiàn)資料)
1.測(cè)定方法的描述,包括分析方法和緩沖溶液的組成信息。
2.原料藥的化學(xué)結(jié)構(gòu),分子量,性質(zhì)(酸、堿、兩性或中性)和解離常數(shù)(pKa)。
3.測(cè)試結(jié)果(平均值、標(biāo)準(zhǔn)偏差、變異系數(shù))以表格的形式匯總,不同pH溶液、藥物溶解度(如mg/ml)以及溶解最大規(guī)格需要的介質(zhì)體積。
4.pH-溶解度的曲線圖
(二)高滲透性的數(shù)據(jù)支持(或文獻(xiàn)資料)
1.測(cè)定方法的描述,包括分析方法和緩沖溶液的組成。
2.人體藥物代謝動(dòng)力學(xué)研究(PK),包括設(shè)計(jì)方案和PK數(shù)據(jù)對(duì)應(yīng)的方法。
3.對(duì)于直接滲透性研究方法,需要說(shuō)明所用方法的適用性,包括研究方案的描述,受試者、動(dòng)物和上皮細(xì)胞系的選擇標(biāo)準(zhǔn),供體液里的藥物濃度,分析方法的描述,計(jì)算吸收程度或滲透性的方法等信息。
4.選擇的模型藥物的清單,應(yīng)包含以下數(shù)據(jù):說(shuō)明研究方法適用性的人體內(nèi)的吸收度數(shù)據(jù)(平均值、標(biāo)準(zhǔn)偏差、變異系數(shù)),每個(gè)模型藥物的滲透率值(平均值、標(biāo)準(zhǔn)偏差、變異系數(shù)),每個(gè)模型藥物的滲透性分類,并根據(jù)滲透性數(shù)據(jù)(平均值±標(biāo)準(zhǔn)偏差或95%置信區(qū)間)給吸收程度按照滲透性分類上下限和所選內(nèi)標(biāo)作出標(biāo)示。支持一個(gè)被測(cè)原料藥高滲透性的信息包括:被測(cè)原料藥的滲透性數(shù)據(jù)、內(nèi)標(biāo)(平均值、標(biāo)準(zhǔn)偏差、變異系數(shù))和穩(wěn)定性信息,適當(dāng)?shù)臅r(shí)候包括支持主動(dòng)轉(zhuǎn)運(yùn)機(jī)制的數(shù)據(jù),以及確定被測(cè)原料藥的高滲透性的研究方法。
當(dāng)f2值≥50時(shí),認(rèn)為兩個(gè)物質(zhì)有相似的溶出特性。為了可以使用平均值,則變異系數(shù)(RSD)在第一個(gè)時(shí)間點(diǎn)時(shí)不應(yīng)超過(guò)20%,在其他時(shí)間點(diǎn)不應(yīng)超過(guò)10%。應(yīng)注意當(dāng)使用上述溶出介質(zhì)時(shí),若仿制制劑和參比制劑均能在15分鐘內(nèi)溶出標(biāo)示量的85%及以上,則不必再利用f2法比較其相似性,可認(rèn)為溶出曲線相似。
]]>